李蓉/潘恒/于洋团队解析子宫内膜衰老新机制

近日,来自北京大学第三医院的李蓉/潘恒/于洋团队在Nature Aging杂志上发表题为Endometrial aging is accompanied by H3K27ac and PGR loss的研究论文,基于北京大学第三医院生殖医学中心接受胚胎植入前遗传学检测(PGT-A)整倍体胚胎移植患者的临床数据分析,证实子宫内膜容受性异常是导致高龄患者妊娠率降低的核心要素。
通过CUT&Tag与 RNA-seq 联合测序,提出子宫内膜衰老伴随组蛋白H3K27ac和孕酮激素受体PGR功能异常的新机制。该研究不仅为明确高龄患者子宫内膜容受性受损机制提供新的理论依据,也对临床上建立更加安全、高效的辅助生殖体系具有重要意义。
子宫内膜容受性异常是子宫内膜功能障碍的重要特征之一,其表现为广泛的形态学和分子水平改变。上皮细胞和基质细胞的协同变化对建立子宫内膜容受性,实现子宫内膜与胚胎植入的同步化至关重要。本研究通过收集患者分泌期子宫内膜样本进行相关检测,发现高龄患者子宫内膜腔上皮细胞异常增殖和基质细胞蜕膜化功能紊乱,雌激素受体(ERα)和孕激素受体(PGR)表达水平显著下降。这些发现从组织形态学和分子生物学层面证实了高龄患者子宫内膜容受性障碍的病理基础,为临床诊疗提供了重要理论依据。
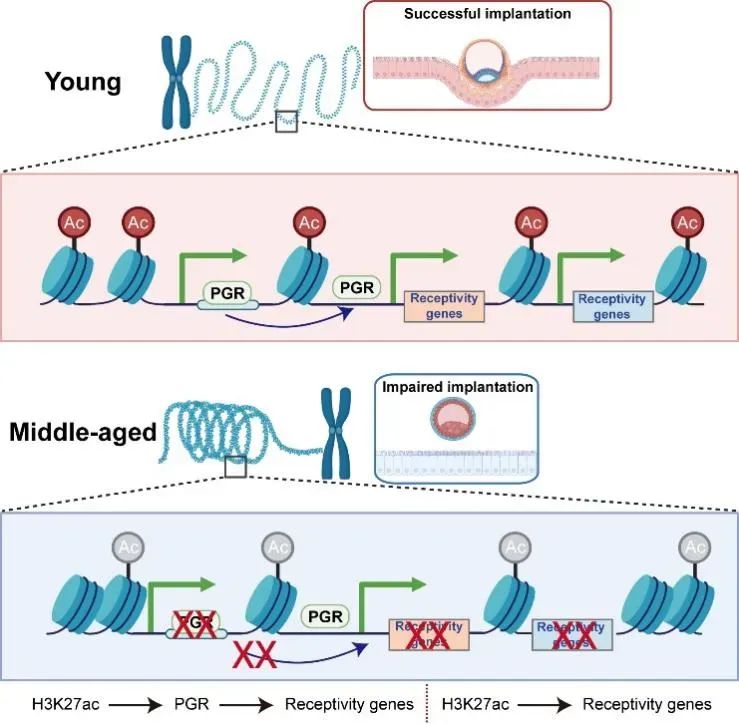
进一步,通过整合分析子宫内膜衰老相关差异基因与组蛋白修饰靶基因的调控网络,提出H3K27ac是调控子宫内膜衰老的关键表观遗传因子。研究显示:(1)高龄患者子宫内膜基质和上皮细胞均呈现显著的H3K27ac修饰水平降低;(2)CUT&Tag测序数据证实H3K27ac直接调控PGR基因的转录活性;(3)体外功能实验表明,通过干预基质细胞H3K27ac可显著抑制PGR表达水平。
北京大学第三医院王越博士后,周平副研究员,单红英博士,刘騱遥博士为本论文的共同第一作者。北京大学第三医院李蓉教授,潘恒研究员,于洋研究员为本论文共同通讯作者。






我要评论 (网友评论仅供其表达个人看法,并不表明本站同意其观点或证实其描述)
全部评论 ( 条)